
Az öregedést meghatározó tényezők: IV. Proteosztázis elvesztése
Az öregedés biológiai hátterét a sejtekben zajló, egymással összefüggő és összetett változások hálózata határozza meg. Carlos López-Otín és kutatócsoportja tizenkét kulcsmechanizmust azonosított, amelyek együttesen formálják az öregedés folyamatait.
A sejtek számos minőségellenőrző rendszert alkalmaznak, hogy biztosítsák fehérjéik működőképességét és stabilitását – ezt a folyamatot proteosztázisnak nevezzük. A proteosztázis (a „proteom” – az összes előállítható fehérje – és a „homeosztázis” – egyensúly – szavak összevonásából) a sejtek azon képessége, hogy a fehérjéket helyesen hajtsák össze, a megfelelő mennyiségben állítsák elő, és szükség esetén kijavítsák vagy lebontsák. Ideális esetben ez az egyensúly folyamatosan fennmarad, ám az életkor előrehaladtával és bizonyos betegségek során ez a rendszer fokozatosan megbomlik. Ebben a cikkben azt vizsgáljuk, hogyan játszik szerepet ez a folyamat az öregedésben és a korral összefüggő kóros állapotok kialakulásában.
|
Először is érdemes jobban megértenünk a fehérjék molekuláris felépítését. Minden fehérje hasonló módon készül. Az első lépés, az úgynevezett transzkripció, a sejtmagban zajlik, és azt jelenti, hogy a DNS-ről – az örökítőanyagunkról – leolvassuk és lemásoljuk a „tervrajzot”.
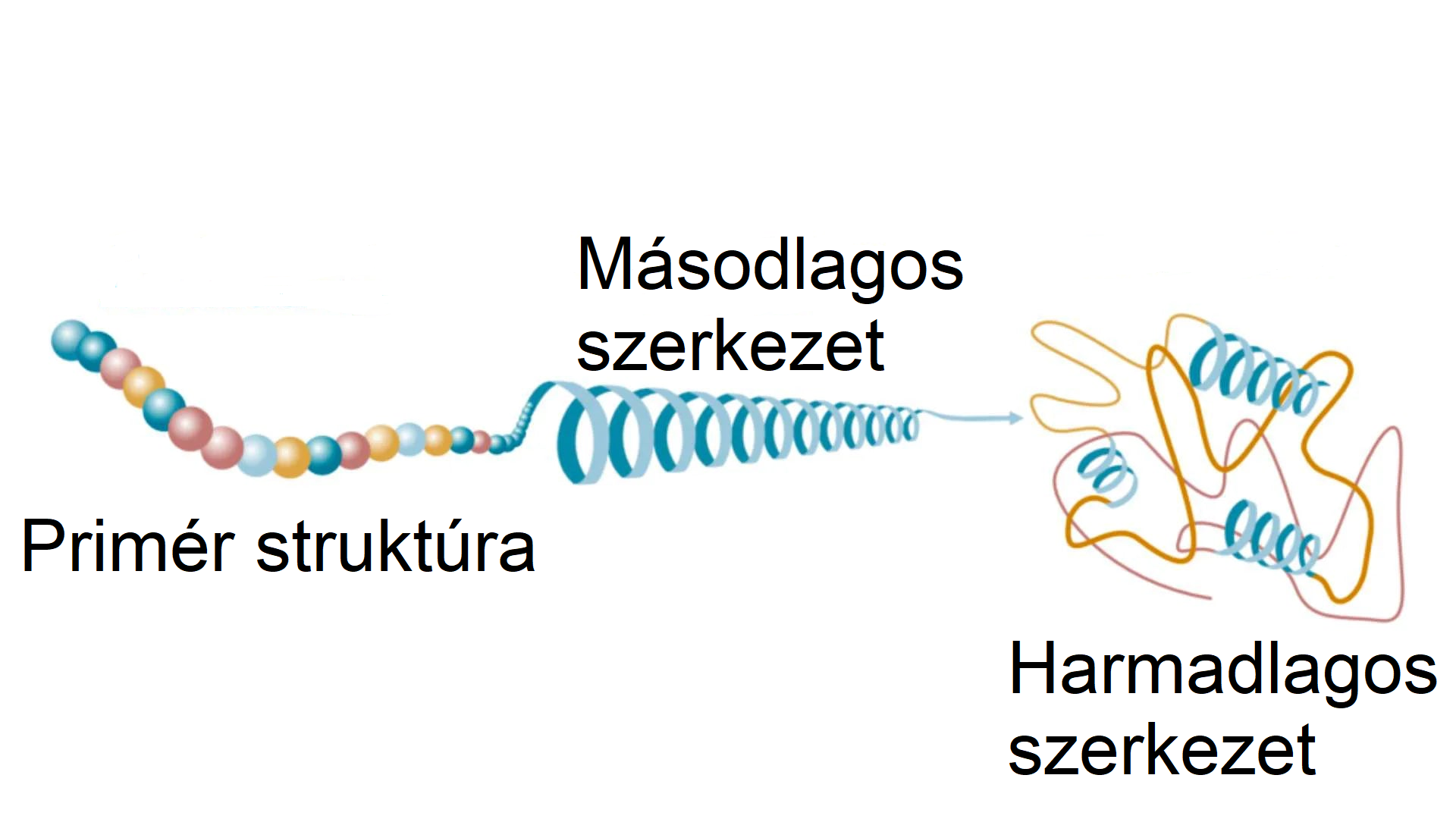
Ezután következik a transzláció, vagyis a „fordítás”. Ekkor a nukleotidokból álló genetikai kód „nyelvét” aminosavak „nyelvére” ültetjük át, vagyis a fehérje az örökítőanyag alapján összeáll. Kezdetben a fehérje egy hosszú, lineáris aminosavlánc, amely egy gyöngysorra emlékeztet – ezt nevezzük elsődleges szerkezetnek (primér struktúra).
Ahhoz, hogy a fehérjék működésbe léphessenek, hajtogatódniuk kell, ami rendkívül összetett folyamat. Először kialakulhatnak ismétlődő, jellegzetes mintázatok, például spirális (alfa-hélix) vagy redőzött (béta-lemez) formák – ezek alkotják a másodlagos szerkezetet. További hajtogatódási lépések során a fehérje háromdimenziós formát ölt (harmadlagos szerkezet), amely lehetővé teszi számára, hogy más fehérjékkel kapcsolódjon és együttműködjön. Egyes esetekben több, különálló fehérjelánc alkot közösen egy funkcionális komplexet – ez a negyedleges szerkezet. |
 |
Chaperonok
Ahogy az ábrán is látható, az aminosav-sorrend – az elsődleges szerkezet – önmagában még nem elegendő a fehérje működéséhez. Ahhoz, hogy a fehérje a szervezetben elláthassa feladatait, több köztes hajtogatódási lépésre van szükség. Csak a harmadlagos szerkezetben rendeződnek az aminosavak háromdimenziós, funkcionálisan aktív formává. Eddig eljutni azonban számos molekuláris kölcsönhatás és kémiai módosítás összehangolt működését igényli.
A folyamat során új kötéseket kell kialakítani, azonban a fehérjehajtogatás rendkívül összetett, és érzékeny a hibákra: akár egyetlen hibás kötés is instabillá vagy működésképtelenné teheti a fehérjét. Éppen ezért a sejtekben kifinomult minőségellenőrző mechanizmusok működnek, amelyek biztosítják, hogy a fehérjék megfelelően hajtogatódjanak.
Az egyik ilyen rendszer a chaperonok csoportja. A „chaperon” szó eredetileg olyan idősebb hölgyet jelentett, aki fiatalabb nőt kísért és felügyelt – egyfajta „illemtanárnő”. A sejtekben a chaperon fehérjék hasonló szerepet töltenek be: ATP-energiát felhasználva segítik az új fehérjék helyes feltekeredését, illetve támogatják a sérült vagy részlegesen denaturálódott fehérjék helyreállítását.
 |
Proteosztázis – hogyan védekezik a szervezet
Becslések szerint a fehérjék 40–80%-a hibásan tekeredik fel, amit többek között UV-sugárzás, nehézfémek, magas hőmérséklet, etanol vagy oxidatív stressz okozhat. Ezek a hatások nemcsak a fehérjék stabilitását bontják meg, hanem a DNS-t is károsíthatják. Külön veszélyforrás az úgynevezett ER-stressz, amikor az endoplazmatikus retikulum – a sejtek „logisztikai központja” – túlterhelődik, így hibás fehérjék halmozódnak fel. Mindez a fehérjék denaturálódásához és működésképtelenségéhez vezethet.
A proteosztázis – a fehérjék szerkezetének és működőképességének fenntartását biztosító rendszer – több mechanizmust is magában foglal az egyensúly helyreállítása érdekében. Káros környezeti hatásokra válaszul a sejtek hősokkfehérjéket termelnek, amelyek chaperonként segítik a hibás fehérjék újrahajtogatását és stabilizálását. Ha ez nem sikerül, a sérült fehérjéket el kell távolítani: ezt a feladatot a proteaszóma látja el, amely az ubiquitin nevű jelzőfehérje segítségével megjelöli, majd aminosavakra bontja a hibás molekulákat.
A proteaszóma és az autofágia – a sejt „belső hulladékkezelő rendszerei” – összehangoltan akadályozzák meg a káros fehérjék felhalmozódását, és biztosítják az intracelluláris fehérjék folyamatos megújulását. Elméletben ezek a mechanizmusok rendkívül hatékonyak, a gyakorlatban azonban nem mindig működnek tökéletesen. |
A fehérjéknél a „ráncosodás”, vagyis a megfelelő hajtogatódás elengedhetetlen a működésükhöz. Idővel viszont a fehérjék hajtogatási rendszere, a proteosztázis, egyre kevésbé működik hatékonyan. Ennek következménye, hogy hibásan feltekeredett vagy egyáltalán fel nem tekeredett fehérjék halmozódnak fel, ami hozzájárul több idős kori betegséghez, például az Alzheimer- vagy Parkinson-kórhoz, illetve a szürkehályog kialakulásához. Ahogy egyre tovább élünk, ezek a betegségek is gyakoribbá válnak.
Az úgynevezett chaperonok – vagyis a fehérjék helyes hajtogatását segítő fehérjék – termelődése az életkor előrehaladtával jelentősen visszaesik. Kutatások arra utalnak, hogy ez a csökkenés hozzájárulhat a rövidebb élettartamhoz. Például genetikailag módosított férgek és legyek, amelyek fokozott mennyiségben állítanak elő chaperonokat, érezhetően tovább élnek. Hasonló mintázat figyelhető meg bizonyos hosszú életű egértörzseknél is, ahol a hősokkfehérjék szintje magasabb az átlagosnál.
Érdekesség, hogy a SIRT1 nevű gén képes fokozni a hősokkreakciót, vagyis támogatja a chaperonok működését. A SIRT1 a szirtuinok családjába tartozik, amelyet gyakran neveznek a „hosszú élet útvonalának” a szervezetre gyakorolt sokrétű, öregedéslassító hatásai miatt. Számos tanulmány erősíti meg a kapcsolatot a chaperonok magasabb szintje és a hosszabb élettartam között.
Az orvosi-biológiai kutatások mára sokat feltártak a proteosztázis működéséről, és egyre több vizsgálat keres kézzelfogható módszereket az életkorral járó proteosztázis-gyengülés lassítására. Az egyik fő irány a chaperonok által közvetített fehérjestabilitás és -feltekeredés serkentése. Egérkísérletekben bizonyos hősokkfehérjék gyógyszeres aktiválása megőrizte az izomműködést, és lassította egyes izombetegségek előrehaladását. Más modellszervezetekben a chaperonok szintjének növelése javította az életkorral összefüggő tüneteket.
Egy másik megközelítés a fehérjebontó rendszerek – például a proteaszóma – működésének fokozása, mivel ezek aktivitása az évek múlásával csökken. Bizonyos enzimek és jelátviteli útvonalak célzott serkentése ezen a téren ígéretes eredményeket mutatott. Szintén fontos a sejtek „nagytakarítását” végző autofágia aktiválása, amely a hibás fehérjék és sérült sejtszerkezetek lebontásának másik fő mechanizmusa.
|
Bár a kutatás még folyamatban van, több beavatkozás is ismert, amelyek ezekre a folyamatokra hatással lehetnek:
Autofágia támogatása: az autofágia – vagyis a sejtek “ön-tisztító” folyamata – serkenthető például időszakos böjtöléssel, kalóriamegszorítással, valamint a spermidin nevű természetes vegyület bevitelével.
Sirtuin-aktiválás: a sirtuinok – az öregedés lassításában szerepet játszó fehérjék – működését fokozhatja többek között a resveratrol és a NAD⁺-szint növelése olyan vegyületekkel, mint a nikotinamid-mononukleotid (NMN) vagy a nikotinamid-ribozid (NR).
Sejtvédelem és a stresszre adott válasz erősítése: polifenolokban gazdag étrend (például bogyós gyümölcsök, zöld tea, kakaó) fogyasztása. |
 |





