
Az öregedést meghatározó tényezők: III. Epigenetikai változások
Az öregedés biológiai hátterét sejtszintű változások összetett rendszere határozza meg. Carlos López-Otín és kutatócsoportja tizenkét ilyen kulcsmechanizmust azonosított, amelyek együttesen formálják az öregedés folyamatait. Ezek közül az egyik terület az epigenetikai változások, vagyis azok a módosulások, amelyek nem magát a DNS-szekvenciát érintik, hanem a gének működésének szabályozását alakítják át.
Az epigenetikai mintázatok fiatal korban szigorúan szabályozzák a sejtek viselkedését. Az életkor előrehaladtával azonban ezek a szabályozási mechanizmusok fokozatosan felborulnak, ami gének túlzott vagy elégtelen működéséhez, és ezáltal a sejtek normál működésének elvesztéséhez vezethet. Ez a „génprogramozási elcsúszás” közvetlen szerepet játszik a gyulladásos folyamatok, a daganatos betegségek, valamint a metabolikus és neurodegeneratív rendellenességek kialakulásában.
|
Míg korábban úgy vélték, hogy minden az örökölt génjeinkben rejlik, ma már világosan látjuk: egészségünket és élettartamunkat nem csupán a genetikai örökségünk határozza meg. A környezeti tényezők és az epigenetikai változások legalább ilyen meghatározó szerepet játszanak abban, hogyan működik a szervezetünk a mindennapok során.
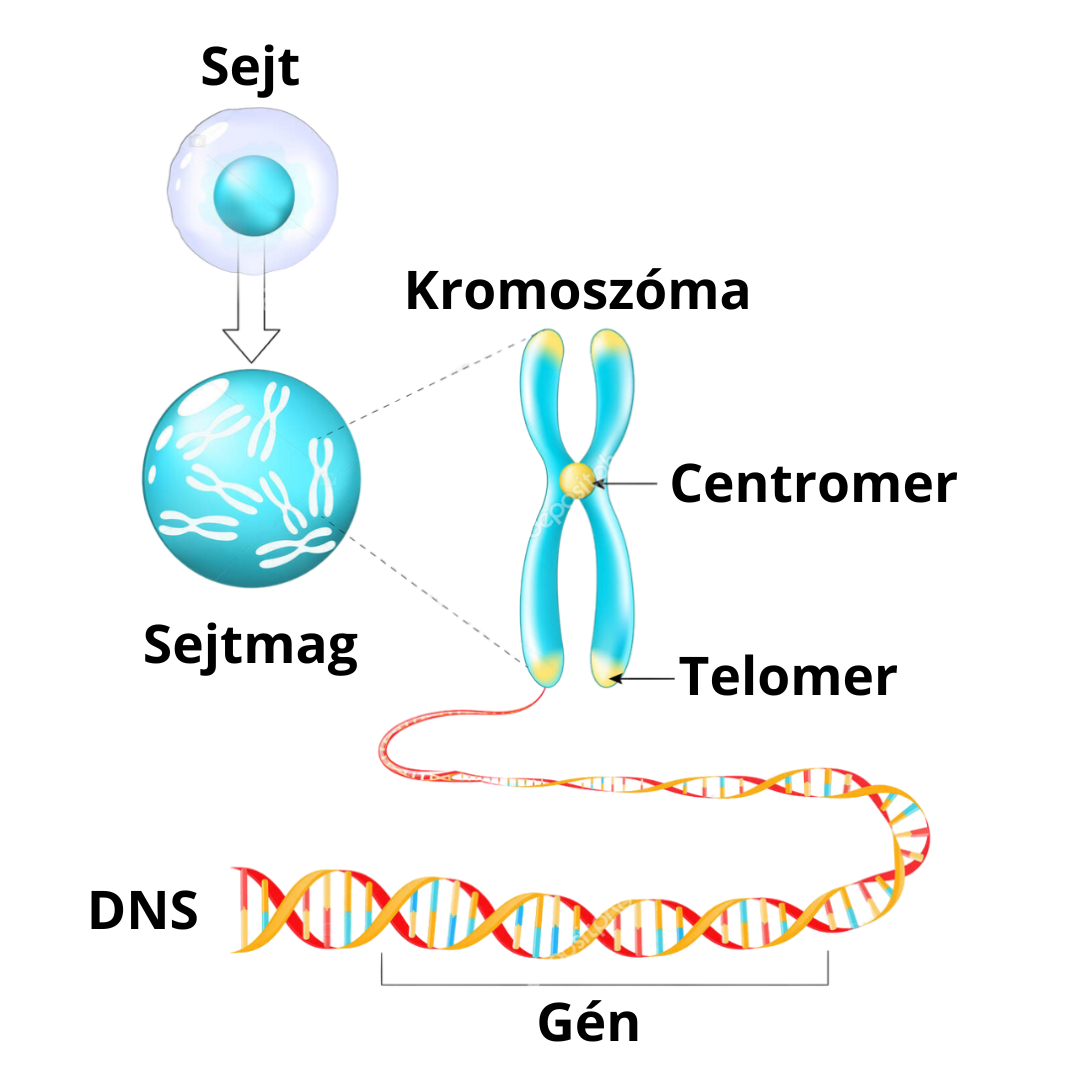
Egy átlagos felnőtt testében hozzávetőleg 100 billió (100 000 000 000 000) sejt található. Ezek többsége tartalmaz sejtmagot, benne a teljes emberi genommal – vagyis azzal az örökletes információkészlettel, amely irányítja a fehérjék termelését, és így formálja testünk szerkezetét és működését.
De vajon hol lép be ebbe a képbe az epigenetika? Az epigenetika szabályozza, hogy a genom mely részei „kapcsolódnak be”, vagyis mely gének fejeződnek ki, és melyek maradnak néma állapotban. Ez a szabályozás létfontosságú szerepet játszik például abban, hogy különböző sejttípusok hogyan működnek, vagy hogy a szervezet miként alkalmazkodik a változó környezeti hatásokhoz. |
 |
Az epigenetika szerepe
Minden sejtünk ugyanazt a genetikai információt hordozza – mégis, ezek a sejtek eltérő szerepeket töltenek be testünkben. Hogyan lehetséges tehát, hogy egyes sejtek izommá, mások bőrré, ideg- vagy májsejtté alakulnak? A válasz a sejtmagban rejlik – pontosabban: az epigenetikában.
Az ember nemcsak genommal, hanem epigenommal is rendelkezik. Míg a genom a DNS-ben kódolt genetikai információ összessége, az epigenom azoknak a kémiai módosításoknak az összessége, amelyek a DNS-hez kapcsolódnak, és mintegy „kapcsolóként” szabályozzák a gének működését. Sok gén mellett található ilyen „kapcsoló”. Ha a kapcsoló BE állásban van, a gén aktív: a benne rejlő tervrajz megvalósul, és a szükséges fehérje előáll. Ha viszont KI állásba kerül, a gén „némává” válik – nem íródik át, így nem is keletkezik belőle fehérje.
Egy szemléletes hasonlat talán még jobban segít megérteni a lényeget: Képzeld el, hogy a DNS-ed egy hatalmas könyv szövege. A könyv azonban olyan terjedelmes, hogy sosem olvasod el elejétől a végéig – mindig csak bizonyos részeket böngészel belőle. A jobb eligazodás érdekében apró Post-it cetliket ragasztasz a fontos bekezdések elejére és végére. Ezek a jelzések felelnek meg az epigenetikai jelöléseknek.
Ezek kémiai szinten például metilcsoportok, amelyek a DNS-hez (vagy a hisztonfehérjékhez) kapcsolódnak. Bár magát a genetikai kódot nem változtatják meg, mégis kulcsfontosságú szerepet játszanak abban, hogy a sejt éppen mely géneket „olvassa le”, és melyeket hagy figyelmen kívül.
És hogy még összetettebb legyen: az „olvasott” szövegrészek nem állandók. Életünk során – a környezeti hatások, táplálkozás, stressz vagy betegségek hatására – folyamatosan változhat, mely gének aktiválódnak, és melyek maradnak inaktívak. Ráadásul az is számít, hogy milyen típusú sejtről van szó – egy idegsejt teljesen más „fejezeteket” olvas, mint például egy bőrsejt.
 |
A gének sokfélesége
Minden gén egy vagy több fehérje tervrajzát hordozza – de ez nem jelenti azt, hogy mindig ugyanazt a fehérjét állítja elő. A magyarázat az úgynevezett alternatív splicing, vagyis alternatív összeillesztés nevű molekuláris folyamatban rejlik.
Ez a mechanizmus lehetővé teszi, hogy egyetlen génből többféle fehérje is létrejöhessen – attól függően, hogy a sejt éppen mely szakaszait használja fel a gén kódolt szakaszainak. Egyes esetekben csak a gén bizonyos részeit „olvassa le” a sejt, más részeket pedig figyelmen kívül hagy, így változatos fehérjék keletkeznek ugyanabból a genetikai forrásból.
Ennek az intelligens biológiai „újraszerkesztésnek” köszönhetően a fehérjék száma jóval meghaladja a gének számát. A tudomány jelenlegi álláspontja szerint az emberi genom körülbelül 20 000–25 000 gént tartalmaz, míg a szervezetünkben megtalálható fehérjék száma 80 000 és 400 000 közöttire tehető.
Ez a szám azonban csak becslés – a proteom, vagyis a teljes fehérjekészlet feltérképezése ma is aktívan kutatott terület. Az eltérő sejttípusok, fejlődési állapotok és környezeti hatások tovább bonyolítják a képet, így a teljes fehérje-összetétel pontos ismerete még várat magára. |
Az epigenetikai rögzülés
Az epigenetika – vagyis az epigenetikai lenyomat – teszi lehetővé, hogy ugyanabból a genetikai állományból különböző sejttípusok alakuljanak ki. Bár minden sejtünk ugyanazzal a DNS-sel rendelkezik, az epigenetikai mintázatok eltérnek, és ezek szabják meg, mely gének aktiválódnak, milyen fehérjék termelődnek, és végül milyen funkciót lát el a sejt. Az epigenetikai módosulások bizonyos esetekben öröklődhetnek is, és bár a terület még fiatal, már most komoly szerepet tulajdonítanak neki több betegség kialakulásában.
A WHO szerint 2016-ban 1,9 milliárd túlsúlyos ember élt a világon, számuk az 1975-ös adatokhoz képest megháromszorozódott. Az elhízás számos betegség, például a cukorbetegség és szívproblémák kockázati tényezője. A mozgáshiány és a rossz étrend mellett az epigenetika is szerepet játszhat ebben a növekedésben. Állatkísérletek arra utalnak, hogy a túlsúlyos szülők utódai örökölhetnek olyan epigenetikai mintázatokat, amelyek hajlamosítják őket a súlygyarapodásra. A jó hír: ez a hajlam megváltoztatható. Az egészséges életmód pozitív epigenetikai jeleket alakíthat ki, így csökkenthető az elhízás kockázata. Azonban további kutatások azonban szükségesek az emberi vonatkozások pontosabb megértéséhez.
|
Epigenetikai változások és az öregedés
Az epigenom – szemben a DNS viszonylag stabil szerkezetével – folyamatosan változik életünk során. Ezek a változások részben a természetes fejlődési folyamatok, részben a környezeti hatások (például stressz, fertőzések vagy táplálkozás) következményei. Az epigenetikai módosulások azonban nem mindig kedvező irányúak.
Számos mechanizmus alakítja az epigenetikai mintázatokat – ezek közül az egyik legfontosabb a DNS-metiláció. Ez a folyamat során metilcsoportok, vagyis kisméretű kémiai jelölők kapcsolódnak a DNS-hez, és befolyásolják a gének kifejeződését. A metilcsoport jelenléte gyakran elnyomja egy gén működését, vagyis megakadályozza, hogy a sejt „leolvassa” a benne tárolt információt. Visszautalva a korábbi hasonlatra: a DNS-metiláció olyan, mintha színes Post-it cetlik jeleznék, mely részeket szeretnénk „elolvasni”, és melyeket nem.
Ezt a folyamatot enzimek, például a DNS-metiltranszferázok végzik, amelyek biztosítják, hogy a metilcsoportok a megfelelő helyekre kerüljenek. És hogyan kapcsolódik mindez az öregedéshez? Friss kutatások szerint az életkor előrehaladtával egyre több metilcsoport kötődik a DNS-hez, és ez fokozatosan megváltoztatja a génkifejeződési mintázatokat. Ezt a jelenséget hasznosítja a Steve Horvath amerikai biogerontológus által kidolgozott epigenetikai óra, közismert nevén a Horvath-óra is. A módszer a DNS-metilációs mintázatok alapján becsüli meg a biológiai életkort. Az epigenetikai korbecslés így kulcsfontosságú biomarkerré vált az öregedéskutatásban és a hosszú élettartamot célzó terápiák értékelésében. |
 |
Az epigenetikai módosulások visszafordíthatók – ez az egyik legnagyobb előnyük, és egyben a legnagyobb lehetőség is. Ez a felismerés új korszakot nyithat az öregedésgátló terápiák, a betegségmegelőzés és a regeneratív orvoslás területén. A kutatások jelenlegi állása alapján egyre valószínűbb, hogy az epigenetikai mintázatok célzott módosítása révén késleltethetőek lesznek az életkorral összefüggő betegségek.
Ma már léteznek epigenetikai órák, mint például a Horvath-óra, amelyek képesek becsülni a biológiai életkort – a jövőben ezek akár személyre szabott egészségtervek alapjai is lehetnek. A valódi kihívás azonban továbbra is a precíziós beavatkozások megvalósítása: olyan eljárások kifejlesztése, amelyek pontosan, mellékhatások nélkül képesek módosítani az epigenetikai jeleket.
Bár a célzott epigenetikai terápiákra még várni, számos életmódbeli tényező már most is képes pozitívan befolyásolni az epigenomot – így hozzájárulhat egészségünk megőrzéséhez és az öregedés lassításához.
Számos kutatás alátámasztja, hogy a kiegyensúlyozott étrend, a túlzott cukor- és zsírfogyasztás kerülése, valamint a kalóriacsökkentés vagy az időszakos böjtölés (pl. intermittent fasting) kedvező epigenetikai hatásokat gyakorolhat a szervezetre. Ezek a táplálkozási tényezők befolyásolhatják a DNS-metilációt, amely kulcsfontosságú mechanizmus az örökítőanyag szabályozásában. Emellett bizonyos mikrotápanyagok – például a folát, a B12-vitamin és a kolin – létfontosságú szerepet játszanak az úgynevezett metilációs folyamatokban, mivel ezek biztosítják a szükséges metilcsoportokat az epigenetikai mintázatok fenntartásához és módosításához.
Az aktív életmód nemcsak a fizikai állóképességet fokozza, hanem epigenetikai úton is hatást gyakorol a génkifejeződésre. A rendszeres testmozgás elősegítheti gyulladáscsökkentő gének expresszióját, miközben csökkentheti a gyulladást és oxidatív stresszt fokozó, illetve anyagcserezavarokhoz kapcsolódó gének aktivitását.
Bizonyos étrend-kiegészítők – például a trimetil-glicin (TMG, betain), kurkumin, rezveratrol és omega-3 zsírsavak – epigenetikailag aktív bioaktív vegyületeknek tekinthetők. Ezen anyagok képesek befolyásolni a DNS-metilációt és a hisztonmódosításokat epigenetikai enzimeken keresztül.
A krónikus stressz epigenetikai változásokat is előidézhet, különösen a kortizolszint tartós emelkedésén keresztül, amely a hipotalamusz–hipofízis–mellékvese (HPA) tengely működését befolyásolja. Kutatások szerint a relaxáció, a jóga, a meditáció és a pihentető alvás hozzájárulhatnak a neuroendokrin és epigenetikai egyensúly helyreállításához.











