
Az öregedést meghatározó tényezők: VII. Elöregedő sejtek
Az öregedés biológiai hátterét a sejtekben zajló, egymással összefüggő és összetett változások hálózata határozza meg. Carlos López-Otín és kutatócsoportja tizenkét kulcsmechanizmust azonosított, amelyek együttesen formálják az öregedés folyamatait. E jellemzők közül a hetedik az elöregedő sejtek jelenléte, vagyis a sejtszeneszcencia. Ez az állapot akkor következik be, amikor bár a leáll a sejtosztódás, azonban eközben a sejt metabolikusan aktív marad. A köznyelvben ezeket a sejteket gyakran „zombisejteknek” nevezik – nem véletlenül: sem teljesen élők, sem valóban halottak.
|
Hayflick-limit és a telomerek
A szeneszcencia (latinul senescere, jelentése: öregedni) alatt a sejtciklus végleges leállását értjük, amely során a sejtek metabolikusan aktívak maradnak, de többé nem képesek osztódni. A fogalom az 1960-as évek elején vált ismertté, amikor Leonard Hayflick és Paul Moorhead kísérleteikben kimutatták, hogy az emberi fibroblasztok sejttenyészetben legfeljebb körülbelül 50 osztódási ciklusra képesek, mielőtt osztódásuk teljesen leáll és a sejtek elöregednek. Ez ellentmondott a korábban uralkodó nézetnek, miszerint a sejtek laboratóriumi körülmények között halhatatlanok.
Hayflick eredményei forradalmi fordulatot hoztak a sejtbiológiában, mivel megmutatták, hogy a halhatatlanság csak a daganatsejtek sajátja. Az osztódások számának ezt a természetes korlátját ma replikatív szeneszcenciának vagy felfedezőjéről Hayflick-határnak nevezzük. Mára az is ismertté vált, hogy a replikatív szeneszcencia fő oka a telomerek — a kromoszómák végén található ismétlődő DNS-szakaszok — fokozatos rövidülése. Ugyanakkor a sejtszeneszcenciát nemcsak a telomer-kopás válthatja ki: DNS-károsodás, oxidatív stressz, vagy krónikus gyulladás szintén kiválthatja ezt az állapotot. |
 |
Mérhető a szeneszcencia?
A telomerek sérülésein túl két további, különösen fontos tényező járul hozzá a sejtszeneszcencia kialakulásához: egyrészt a nem-telomerikus eredetű DNS-károsodások, másrészt a DNS-en található INK4/ARF lókusz aktivációja. Mindkét mechanizmus szoros kapcsolatban áll a kronológiai öregedéssel, és önmagában is képes kiváltani ezt az állapotot — ezt több kísérleti modell is alátámasztotta.
A sejtszeneszcencia jelenléte közvetlenül nem mérhető, ugyanis nem áll rendelkezésre olyan laboratóriumi paraméter, amely például vérvétel során számszerű értéket adna e jelenségről. Éppen ezért a kutatók ún. helyettesítő markereket alkalmaznak, amelyek a szeneszcencia közvetett kimutatására szolgálnak.
Egy 2009-ben publikált állatkísérlet során a kutatók ezen markerek alapján számszerűsítették a szeneszcens sejtek előfordulását egerek különböző életkoraiban. Az eredmények szerint a fiatal egyedekben a szeneszcens sejtek aránya átlagosan 8% körül mozgott, míg az idős állatokban ez az arány megközelítette a 17%-ot. Szervspecifikus vizsgálatok kimutatták, hogy a bőrben, a tüdőben és a lépben jelentős növekedés tapasztalható volt, ugyanakkor a szív, a vese és az izomszövet esetében nem mutatkozott szignifikáns változás. Ez arra utal, hogy a sejtszeneszcencia mértéke és hatása szervenként eltérő.
 |
MoleQlar One - Napi Longevity komplex
A hosszú és egészséges élet nem szerencse kérdése, hanem a mindennapokban meghozott tudatos döntések eredménye. A MoleQlar One egyetlen tasakban egyesíti a legmodernebb, hosszú élettartamot támogató molekulákat, valamint esszenciális vitaminokat és ásványi anyagokat.
A formula a Carlos López-Otín és kutatócsoportja által leírt, a szervezet öregedését meghatározó 12 alapfolyamat mindegyikére fókuszál. Kutatások igazolják, hogy ezeknek a sejtszintű mechanizmusoknak a célzott támogatásával lassítható az öregedés üteme, és hosszabb ideig megőrizhető a testi és szellemi vitalitás.
A MoleQlar One egyedülállóan széles spektrumú, 31 összetevőt tartalmazó összetételével kifejezetten úgy lett megalkotva, hogy átfogó támogatást nyújtson ezeknek a kritikus sejtszintű folyamatoknak, ezzel segítve a hosszú, aktív és egészséges élet elérését. |
Öregedés és sejtszeneszcencia
Ma már jól dokumentált, hogy az életkor előrehaladtával a szeneszcens sejtek száma fokozatosan növekszik — ezt a jelenséget számos kutatás megerősítette. De vajon miért történik ez? Egyrészt több szeneszcens, azaz „leállított” sejt keletkezhet, másrészt csökkenhet azok hatékony eltávolítása. Valójában a két folyamat párhuzamosan zajlik. Fontos azonban elkerülni azt a leegyszerűsített következtetést, hogy a szeneszcens sejtek puszta jelenléte önmagában az öregedés „főellensége” lenne. A biológiai összefüggések ennél jóval összetettebbek.
A sejtszeneszcencia egyik evolúciósan konzervált célja feltehetően nem az öregedés előidézése, hanem a károsodott sejtek szaporodásának megelőzése és azok eltávolításának elősegítése az immunrendszer révén. A DNS-károsodás, amelynek jelenlétét gyakran markerként használják a szeneszcencia azonosítására, éppen ezt a védekező mechanizmust indíthatja be. A szeneszcencia tehát kezdetben hasznos adaptív válaszreakció: egyfajta sejtbiológiai „vészfék”, amely segít fenntartani a szöveti integritást, sőt akár daganatmegelőző szerepe is lehet.
Ehhez a pozitív hatáshoz azonban elengedhetetlen egy jól működő sejtpótló (regenerációs) rendszer, amely képes a szeneszcens sejtek eltávolítására és az elvesztett sejtek pótlására. Az életkor előrehaladtával azonban ez a rendszer fokozatosan veszít hatékonyságából. A regenerációs kapacitás csökkenése miatt a szeneszcens sejtek felhalmozódnak, ami krónikus szöveti károsodást, gyulladást és végső soron az öregedési folyamat felgyorsulását idézheti elő.
Fontos kiemelni, hogy önmagában a szeneszcens sejtek jelenléte még nem feltétlenül káros. Sokkal nagyobb szerepe van annak, hogy ezek a sejtek mit bocsátanak ki környezetükbe. Ez a sejtek által termelt és kiválasztott molekulák összessége, az ún. szekretom, mely különösen gazdag gyulladáskeltő citokinekben, proteázokban és egyéb szövetromboló anyagokban. Ezt a jelenséget a tudomány szeneszcenciával társult szekréciós fenotípusként (Senescence-Associated Secretory Phenotype, SASP) írja le. A SASP kulcsszerepet játszik a környező sejtek működésének befolyásolásában, a szöveti gyulladás fenntartásában, és hozzájárulhat különféle életkorral összefüggő betegségek kialakulásához.
Nemcsak a DNS-károsodás, hanem a túlzott mitogén jelátvitel is kiválthatja a sejtszeneszcenciát. Ezt a sejtek stresszként érzékelik, és védekezésképpen leállítják az osztódást, hogy megelőzzék a tumorképződést.
A folyamat kulcsszereplője az INK4a/ARF-lókusz, amely olyan szabályozófehérjéket kódol, mint a p16^INK4a. Ennek expressziója az életkor előrehaladtával növekszik, és számos életkorral összefüggő betegséghez köthető. Hasonló szerepet játszik a p53 is, amely szintén központi szabályozója a sejtciklus blokkolásának és a szeneszcenciának.
Bár mindkét fehérje erős daganatellenes hatással bír, aktiválódásuk hosszú távon hátrányos lehet. Állatkísérletek azt mutatják, hogy túlzott aktivitásuk felgyorsíthatja az öregedést, míg mérsékelt szintjük hozzájárulhat a hosszú élettartamhoz. E kettős szerepük jól példázza az öregedés és daganatmegelőzés közti finom egyensúlyt.
|
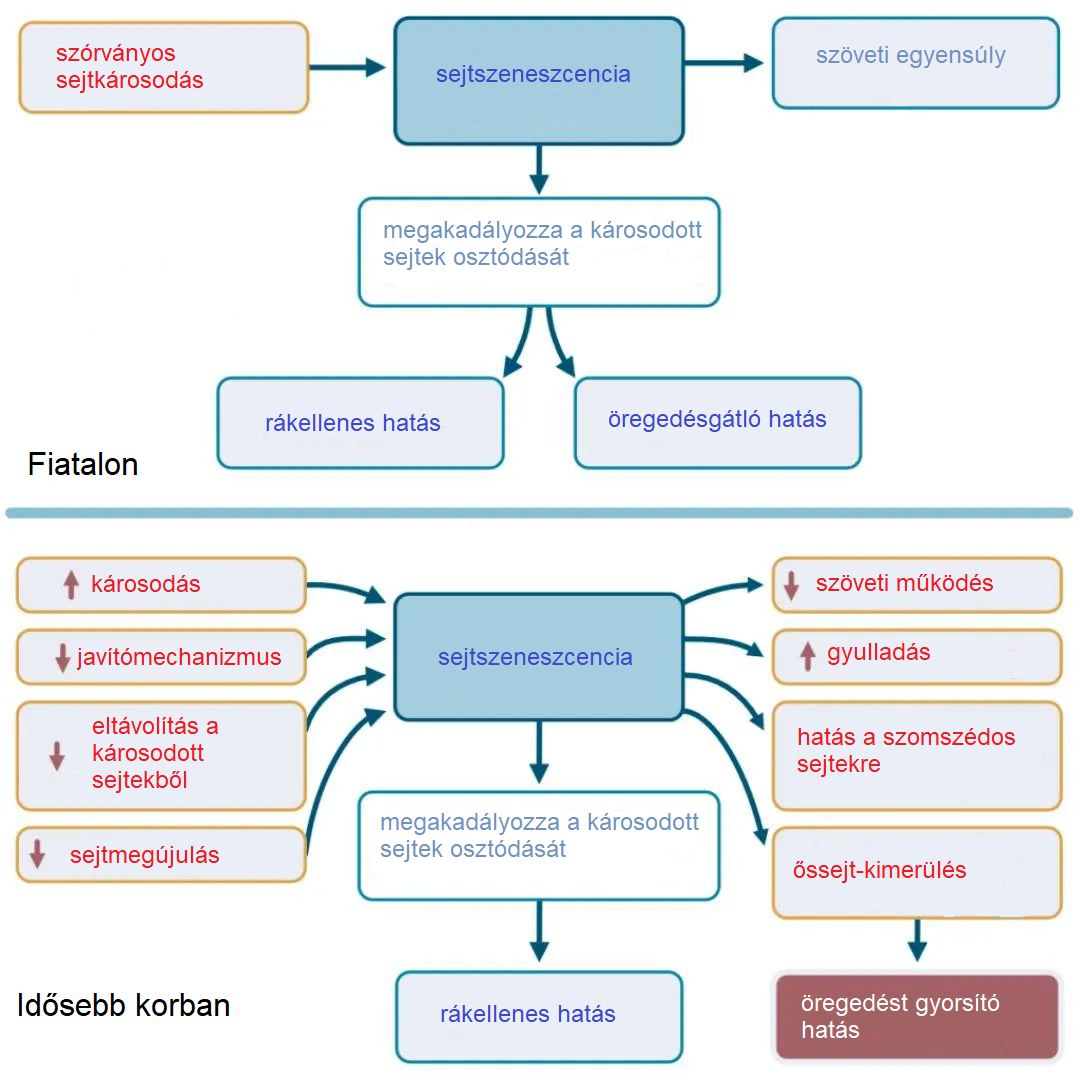
A sejtek szeneszcens állapotba lépnek válaszul különféle károsodásokra, hogy megelőzzék a hibás sejtek további osztódását. Ez a mechanizmus különösen fontos a daganatképződés megelőzésében, ezért fiatal szervezetben a szeneszcencia adaptív, védőreakciónak tekinthető.
Azonban az életkor előrehaladtával a regenerációs kapacitás csökken, így a szeneszcens sejtek már nem tudnak megfelelően eltávolítódni, és fokozatosan felhalmozódnak. Ezek a leállított sejtek gyulladást keltő anyagokat választanak ki, zavarják a környező sejtek működését, és hozzájárulhatnak különféle időskori betegségek kialakulásához.
A megoldás kulcsa az egyensúlyban rejlik: míg fiatal korban a sejtszeneszcencia a szervezet egyik legfontosabb védelmi mechanizmusa, addig idősebb korban – amikor a szeneszcens sejtek eltávolítása már nem történik hatékonyan – ezek a sejtek felhalmozódhatnak, hozzájárulva a krónikus gyulladáshoz, szöveti károsodáshoz és funkcióvesztéshez. |
 |
Az időskori egészség megőrzésében egyre nagyobb figyelem irányul a szenolitikumokra – vagyis olyan terápiás szerekre, amelyek szelektíven képesek eltávolítani a feleslegessé vált szeneszcens sejteket. Az egyik ígéretes jelölt ebben a kategóriában a spermidin, egy természetes poliamin, amely az autofágiát serkentve közvetett módon hozzájárulhat a szeneszcencia által érintett sejtek eltakarításához, és ezáltal lassíthatja az öregedést.









