Az öregedést meghatározó tényezők: II. Telomerek kopása
Az öregedés hátterében sejtszintű folyamatok bonyolult hálózata áll. Carlos López-Otín és munkatársai tizenkét ilyen alapmechanizmust azonosítottak, amelyek együtt formálják az öregedés biológiai mintázatát. Ezek közül az egyik meghatározó tényező a telomerek kopása, amely a sejtek ismétlődő osztódása során zajlik, és jelentős hatással van a szövetek regenerációs képességére. A telomerek kopása idővel a sejtek működésének leállásához, valamint számos öregedéssel összefüggő betegség kialakulásához vezethet. Az alábbi cikkben részletesen bemutatjuk a telomer-rövidülés mögötti biológiai folyamatokat, és áttekintjük azokat a lehetőségeket, amelyekkel ez a folyamat lassítható.
|
A telomerek
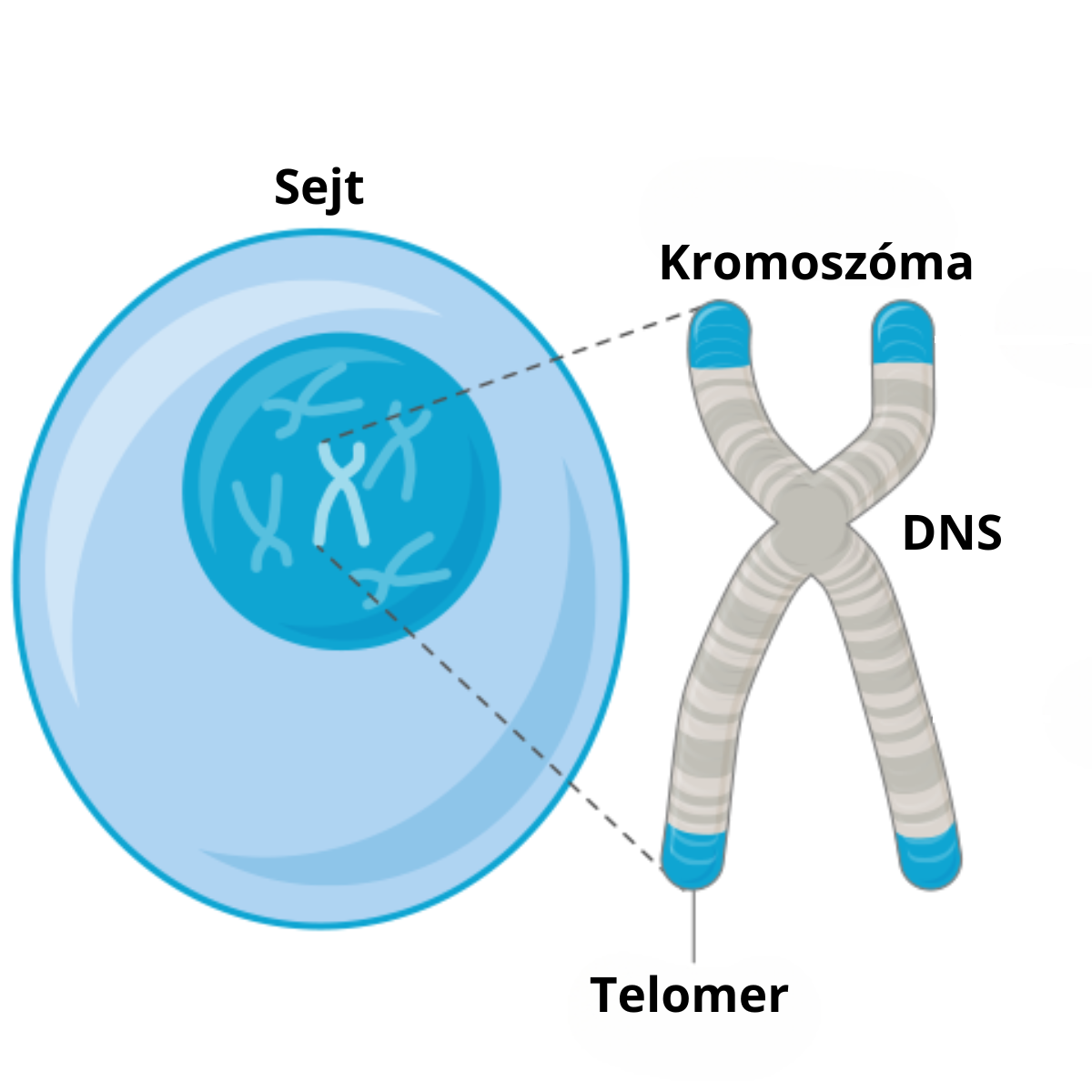
Testünk szinte minden sejtjének sejtmagjában megtalálható a DNS, vagyis a dezoxiribonukleinsav, amely az öröklött genetikai információ hordozója, és 23 pár kromoszómából áll. A kromoszómák végén helyezkednek el a telomerek — speciális, nem kódoló szakaszok, amelyek nem fehérjéket vagy más funkcionális molekulákat hoznak létre, hanem védelmi szerepet töltenek be: megóvják a DNS-t a károsodástól és a sejtosztódás során bekövetkező veszteségektől.
|
 |
Telomeráz
Léteznek bizonyos sejtek, amelyek mentesek a telomerek rövidülésének problémájától. Ennek kulcsa egy különleges enzim, a telomeráz, amely képes újraépíteni a telomereket, gyakorlatilag „halhatatlanságot” biztosítva a sejtek számára. Felmerül a kérdés: ha ezt az enzimet minden sejtben aktiválni tudnánk, vajon megállíthatnánk az öregedést? A válasz azonban összetettebb — a természet okkal korlátozta a telomeráz működését.
Sejtjeink DNS-ét folyamatosan érik külső és belső károsító hatások, amelyek mutációkhoz vezethetnek. Bár a sejtek fejlett javítómechanizmusokkal rendelkeznek, nem minden hibát képesek korrigálni. És itt rejlik a veszély: ha egy hibás, mutált sejt telomerázhoz jutna, korlátlanul osztódhatna — ez a folyamat a daganatos sejtek szaporodásának alapja. A telomeráz tehát kétélű fegyver: miközben potenciálisan lassíthatja az öregedést, fokozhatja a rák kialakulásának kockázatát.
A telomerázt termelő sejtek — például az őssejtek és a csontvelősejtek — a szervezet szigorúan ellenőrzött, védett környezeteiben találhatók. Ezek a sejtek alapvetőek a szövetek megújulásához és az egészséges működés fenntartásához. Különleges védelmi rendszereik révén ellenállóbbak a mutációkkal szemben, így képesek hosszú távon is fenntartani a regenerációt, anélkül hogy daganatkockázatot jelentenének.
A telomeráz jelenléte tehát elengedhetetlen bizonyos sejtek élettani működéséhez, ugyanakkor szigorúan szabályozott mechanizmusok irányítják annak aktiválását. A jövő öregedéskutatásának egyik legnagyobb kihívása éppen ebben áll: megtalálni azt az egyensúlyt, amely lehetővé teszi az élettartam növelését anélkül, hogy növelnénk a daganatos betegségek kockázatát.
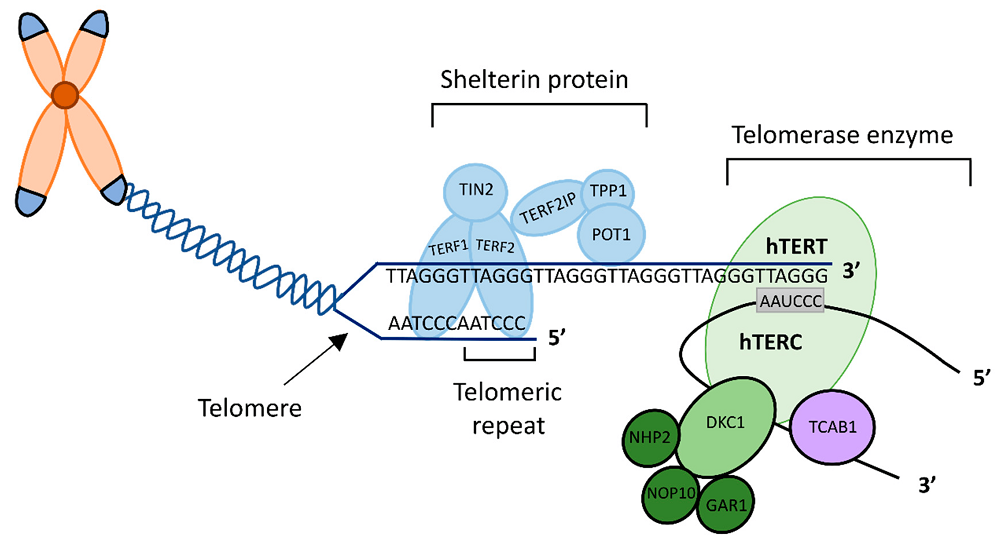 |
Shelterin
Ahogyan sok más esetben, a természet itt is gondoskodik a sejtek védelméről: az emberek – és sok más élőlény – rendelkeznek egy különleges mechanizmussal, amely a telomerek épségét őrzi. Ezt a védelmi rendszert a shelterin nevű fehérjekomplex biztosítja, amely közvetlenül a telomerekhez kötődve védi azokat a sejtek saját javítómechanizmusaitól. Ez a „molekuláris pajzs” kulcsszerepet játszik a kromoszómák stabilitásának fenntartásában, és segít megelőzni a sejtek idő előtti degenerációját – feltéve, hogy működése zavartalan.
Bár a shelterin hatékony védelmet nyújt, a telomerek így sem teljesen védettek a DNS-károsodásokkal szemben, különösen a genetikai instabilitásból eredő hatások ellen. Mivel a shelterin elrejti a telomereket a sejtek javítófolyamatai elől, az itt keletkező sérülések gyakran nem kerülnek kijavításra. Ez elsőre aggasztónak tűnhet, hiszen a felhalmozódó hibák olyan folyamatokat indíthatnak el, mint a szeneszcencia – amikor a sejt már nem osztódik, de nem is pusztul el – vagy a programozott sejthalál (apoptózis).
Szerencsére a telomer régiók nem tartalmaznak génkódoló információt, így az itt bekövetkező DNS-károsodások általában kevésbé veszélyesek a sejtműködés szempontjából, mint a kromoszómák más, fehérjét kódoló szakaszain. Ez azt jelenti, hogy a telomerek sérülése ritkábban okoz közvetlen funkcionális problémát, noha idővel hozzájárulhat a sejtek öregedéséhez és működési zavaraihoz. |
A rövid telomerek és a korai halálozás kockázata
A szövetek regenerációs képességének csökkenése komoly egészségügyi kihívásokat jelent, és kutatások kimutatták, hogy a rövid telomerek jelentősen növelik a korai halálozás kockázatát. Ez rávilágít arra, hogy a telomerek hossza nem csupán az öregedés természetes velejárója, hanem alapvető szerepet játszik az egészség és a hosszú élettartam fenntartásában. Mindez hangsúlyozza a telomeráz enzim és a shelterin fehérjekomplex megfelelő működésének fontosságát, hiszen ezek elengedhetetlenek a sejtek és szövetek egészségének megőrzéséhez, valamint az öregedéssel összefüggő betegségek megelőzéséhez.
Mit tehetünk?
Miközben a tudomány a telomerhosszabbító terápiák lehetőségeit kutatja, érdemes áttekinteni azokat a módszereket is, amelyek bizonyítottan hatékonyak az emberi szervezetben.
A magnézium-anyagcsere kiemelten fontos szerepet játszik a telomerek egészségének megőrzésében. Ez az esszenciális ásványi anyag számos létfontosságú biológiai folyamatban vesz részt, és elengedhetetlen a telomerek stabilitásához és megfelelő működéséhez. Kutatások kimutatták, hogy alacsony magnéziumszint, különösen magas homociszteinszinttel együtt, gyorsítja a telomerek rövidülését.
Ha a telomerek és az ún. másodlagos növényi vegyületek kapcsolatát vizsgáljuk, hamar eljutunk a sirtuinokhoz — ezekhez a fehérjékhez, amelyeket gyakran a „hosszú élet génjeiként” emlegetnek. A sirtuinok aktiválása többféle módon történhet: az egyik legismertebb természetes serkentőjük az időszakos böjt, amely klinikai vizsgálatok szerint jelentősen növeli ezeknek a fehérjéknek a szintjét. Emellett bizonyos fitonutriensek, például a rezveratrol, szintén hatékonyan támogatják a sirtuinok működését.
A magas sirtuinszint több szinten is kedvezően hat a sejtműködésre: segít megőrizni a telomerek stabilitását, védi a DNS-t, és szabályozza az epigenetikai folyamatokat, vagyis a gének működését anélkül, hogy megváltoztatná azok szerkezetét.
Mindez egyértelműen rámutat arra, hogy az életmódbeli tényezők — mint a megfelelő étrend, az időszakos böjt és a célzott tápanyagbevitel — kulcsszerepet játszhatnak a sejtek öregedésének lassításában, és hozzájárulhatnak egy hosszabb, egészségesebb élet megvalósításához.












